定期通信第66号は、2025年6月12日に、東京農業大学世田谷キャンパス内横井講堂で開催された「2025年度第1回講演会」の聴講録です。講演の概要を簡潔に取りまとめ、数枚のスライドを挿入して、ご講演をいただきました、渡邉敬浩先生、今城敏先生、山田友紀子先生に監修をしていただいたものです。
会誌「食の安全と微生物検査」第15巻第1号の資料を合わせてご覧ください。
講演会の動画記録を会員限定ですが、Vimeoでアーカイブ配信しています。利用方法については、当法人のホームページの会員専用ページをご覧ください。
テーマ:食のリスクマネジメントにおける国際整合性
●講演1
食品規格の実効に必要な分析の国際整合 (渡邉 敬浩 先生)
●講演2
食品企業における国際整合性の意義(今城 敏 先生)
●講演3
国際的に合意された化学的食品安全の枠組み―汚染物質と残留農薬を例として-(山田 友紀子 先生)
講演1
食品規格の実効に必要な分析の国際整合
渡邉 敬浩
国立医薬品食品衛生研究所 安全情報部第1室長
国立医薬品食品衛生研究所 安全情報部第1室長
※注意事項:講演に先立ち、渡邉敬浩先生から以下のお願いとお知らせがありましたので、この聴講録におきましても、お読みいただく場合には、その点にご配慮いただきますようお願い申し上げます。
おねがい
本講演の内容には、個人の考えや意見が含まれます。あらかじめご承知おきください。
業務管理要領改訂案と内部品質管理の一般ガイドライン案は、H29~R1年度に実施した厚生労働科学研究により開発しました。 (H29年度分担報告書:
https://mhlw-grants.niph.go.jp/system/files/2017/173031/201723024A_upload/201723024A0004.pdf)
その後の検討会による議論を経て、R3年度に最終化されました。 本講演(資料)では、検討会が最終化し厚生労働省に勧告した案(最終案)の一部を引用しています。現在、この最終案を基礎として公にするための文書(通知)の作成が検討されていると聞いています。
1. 国際整合における課題と食品安全の現状
「国際整合(international harmonization)」におけるharmonizationは、日本語では「調和」と「整合」の二つの意味合いを持つ。「調和」には能動的な意味合いがあり、「整合」には受動的な意味合いがあると考えている。食品安全の多くの分野において、残念ながらわが国は「調和」に貢献できていない。専門家会合などで「調和」された原理原則や考え方に、何とか追いつこうと「整合」する努力をしているのが現状である。
食品規格の実効に必要な要素
食品規格を実効性のあるものにするためには、「サンプリングと分析」、そして判定を要素とする「検査」、および「品質保証」が不可欠である。
「サンプリング」とは、ある食品が特定の集団を形成している場合に、その集団の特性を正確に反映し、代表となる食品を抜き出す行為を指す。サンプリングの対象はロットであり、多くの場合、均質であることを前提とする。また、集団の特性を把握するという目的を達成できる方法(サンプリングプランとサンプリング手順)を選択しなければならない。
「分析」とは、「あるもの」が持つ多様な特性の中から、「知りたい特性」のみを選択し、それを明らかにするための行為である。食品分析においては、「あるもの」は食品、「知りたい特性」は、主に以下の3点が基本となる。
- 食品そのものの特性
- 食品を構成する成分の特性
- 食品の製造から消費の間に付随するものの特性
先述のとおり、「検査」は、サンプリング、試験(分析)、判定の3つの要素で構成される。原理的に完全に間違いのない検査はありえない。ここで言う「間違い」とは、適合しているロットを誤って不適合と判定する確率、あるいは逆に適合していないロットを誤って適合と判定してしまう確率があることを指す。
微生物検査の場合、流通後に増殖する可能性があるため、量よりも質的な管理が重要である。そのため、最終製品の検査よりも、製造工程における衛生管理がより有効なリスク管理手段となる。食品衛生においては、規格値と検査(サンプリング、分析、判定基準)が連動して設定される必要がある。
「品質保証」とは、品質要求を満たした分析結果を得る能力があることを証明し、実際にそのような分析結果が得られていることを合理的に説明可能にするために必要な一連の取り組みを指す。分析結果の品質は、サンプリング法及び分析法の性能、試験所の品質保証への取り組みによって決まる。
多数の分析結果が必要か、精確性が高い結果が必要かなど、分析の目的によって分析結果の品質に対する要求水準は異なる。そのため、分析結果の品質を継続的にモニター・レビューし、必要に応じて見直しと改善を行う必要がある。

2. 食品規格(分析)の国際整合のためのプラットフォーム
コーデックス委員会は、国際連合食糧農業機関(FAO)と世界保健機関(WHO)の管理下に設置された国際政府間組織である。コーデックス委員会では、食品規格や衛生規範などの文書が策定され、それらの総称が食品法典(コーデックスアリメンタリウス)であると説明されている。食品安全に関しては、コーデックス委員会が策定する規格、基準、規範、指針などの各種文書が国際標準となる。食品事業者等はコーデックス文書に直接従う義務はないが、結果としてコーデックス文書との整合が求められる。
コーデックスにおける分析法は、以下の4種類に分類される。
- 定義分析法(Type I)
- 参照法(Type II)
- 代替法(Type III)
- 暫定法(Type IV)
微生物分析法の多くはType Iに分類される。Type Iの分析法は、特定の分析条件下で許容される唯一の分析結果を決定するものとされている。そのため、微生物分析において、分析原理(特定の培地、一定の温度、及び時間での培養など)の変更はできない。

3. 食品規格の実効に必要な分析の国際整合
試験所の能力と品質保証に関する国際標準であるコーデックスガイドライン・CXG27には4つの必要事項がある。そのうちのISO/IEC 17025の基準遵守は、日本の食品検査における品質保証関連通知である現在の業務管理要領では満たされていない。
そのため、適正な検査を実施するためにも、国際整合を考慮した業務管理要領の改訂や内部品質管理(IQC)ガイドラインの開発が課題となっている。妥当性確認とは、意図する特定の用途に対して個々の要求条件が満たされていることを調査によって確認し、客観的な証拠を用意することを指す。
妥当性確認された分析法の適用可能性を判断するには、不足するデータを補う経験や情報も必要である。また、運用開始後もIQCと技能試験を通じて、分析結果の品質をモニターし続けることが必要となる。CCMAS(コーデックス委員会分析・サンプリング部会)では、Type I分析法への同等性を評価するためのガイドライン作成について議論されたが、合意には至っていない。Type I分析法では同等の分析法は認められず、コーデックスで決められた分析法を選択するしかない。

Q&A
Q1-1諸外国によって食の習慣、環境、考え方が異なる中で、国際整合性の基準をどのように決めるのがよいか?
A1-1コーデックスをプラットフォームとして国際整合を進めていきたいと考えている。コーデックスは、原理原則や考え方を示す標準を作成しているという認識である。コーデックスは世界標準だが、日本の国益を考慮し、日本に寄り添った国際整合ができれば、政府、企業、消費者のいずれにとっても良い結果になると考えている。
講演2
食品企業における国際整合性の意義
今城 敏
食品安全技術センター 代表
食品安全技術センター 代表
食品のグローバル化が進む現代において、食品安全マネジメントにおける国際的な整合性の確保は、企業の持続的発展と消費者の信頼獲得に不可欠な要素である。今城先生は本講演において、「国際的な共通認識」から「日本の食品安全行政」、「HACCPの義務化」、「国際的枠組みへの適合」について解説された。
1. 食品安全の国際的潮流と日本の現状
現在、食品安全におけるリスク管理の重要性は国際的な共通認識となっており、コーデックス委員会が策定する各種国際基準でも「科学的根拠に基づくリスク分析」が強調されている。「後始末より未然防止」という予防的アプローチが国際的に重視されている。
日本では、2021年6月1日より改正食品衛生法が全面施行され、HACCPに沿った衛生管理、すなわち「食品安全確保のためのリスクに基づくアプローチ」が原則としてすべての食品等事業者に義務付けられた。
しかし、HACCPだけではアレルギー表示などの新たな食品安全課題への対応が不十分な場合があり、近年のグローバルな食品安全管理の潮流は、より包括的かつ予防的なアプローチへと進んでいる。企業は新たな食品安全リスクに対応するため、ISO規格やGFSI承認スキームなど、国際的枠組みへの適合(食品安全マネジメントの強化)を求められている。
2. BtoBにおける食品安全の取り組みと課題
HACCPの課題として、「アレルギー表示対応などの新たな食品安全課題への対応が不十分であり、新たな食品安全リスクに対応するにはさらなる管理手法が必要」という点がある。
グローバルサプライチェーンにおいて、企業間(BtoB)取引における食品安全確保は不可欠である。サプライヤーの管理体制が自社製品の安全性に直結するため、取引先の食品安全管理水準や監査結果の共有、取引先間の情報の透明性確保などが重要となる。BtoB取引における主な課題は以下の通りである。
-
評価方法の標準化
評価方法が標準化されていないため、サプライヤーの負担が増大し、改善が困難となる。 -
情報共有システムの構築
リアルタイムで正確な情報共有が必要だが、問題発生時の迅速な対応が困難である。 -
国際的基準への適合性
グローバルスタンダードへの準拠が必要であり、FSSC22000やSQF導入の有効性が問われている。
3. 食品安全認証制度の概要
食品安全認証制度は、特定の食品安全基準を企業が満たしているかを第三者機関が審査・証明する仕組みである。食品安全認証の意義としては、「消費者や取引先への安全保証」、「ブランド価値の向上」、「BtoBにおける信頼獲得」がある。
現在、世界的に広く認知・活用されている主要な食品安全認証制度として、FSSC22000(オランダ)、SQF(アメリカ)、BRCGS(イギリス)、IFS(ドイツ・フランス)、JFS-C規格(日本)などがある。これらはエリアやセクターごとに発展した制度であるが、いずれもGFSI(Global Food Safety Initiative:世界食品安全イニシアチブ)によって承認されたスキームであり、国際的に整合性が確保されている。

4. GFSIの成果と今後の展望
GFSIは、世界的な食品安全に関する企業団体であり、食品安全基準の整合化や監査手法の改善を推進している。グローバル食品サプライチェーンの安全確保や食の危機発生時の迅速な対応力強化などを目的とし、具体的には以下のような活動を行っている。
- 食品安全認証スキームの評価・承認
- 食品安全文化の普及
- 世界の食品安全水準の向上への貢献
これまでにGFSIが達成したこととしては、「認証の同等性確立」、「業務の重複削減」、「コスト効率の向上」、「食品安全文化の普及」がある。
5. GtoGの影響と米国食品安全行政
GtoG(Government to Government)がもたらす影響としては、「政府間協定の重要性」、「輸出入要件の整合」、「企業への影響」がある。
GtoGの政府間協定は重要であり、交渉によっては相手国が有利で自国が不利になるケースもある。そのような場合、いかに自国の法律を根拠とするか、また国際的協調性(コーデックスなど)を活用して輸出入先国の食品安全要件との整合性を確保し、食品安全基準遵守による輸出入の円滑化を図るかが重要となる。
食品安全に関する新たな法規制の導入は企業にとって喫緊の課題となっており、法規制への迅速な対応はブランドイメージの向上や新たな市場開拓につながる。また、迅速な準拠は他社に先駆けて新しい製品やサービスを市場に投入することを可能にし、大きな先行者利益を得られる。このように、法的要求事項に先駆けて適切に対応できれば、消費者からの高い信頼を勝ち得て、長期的な事業基盤の強化につなげることができ、大きな競争優位性を得ることができる。
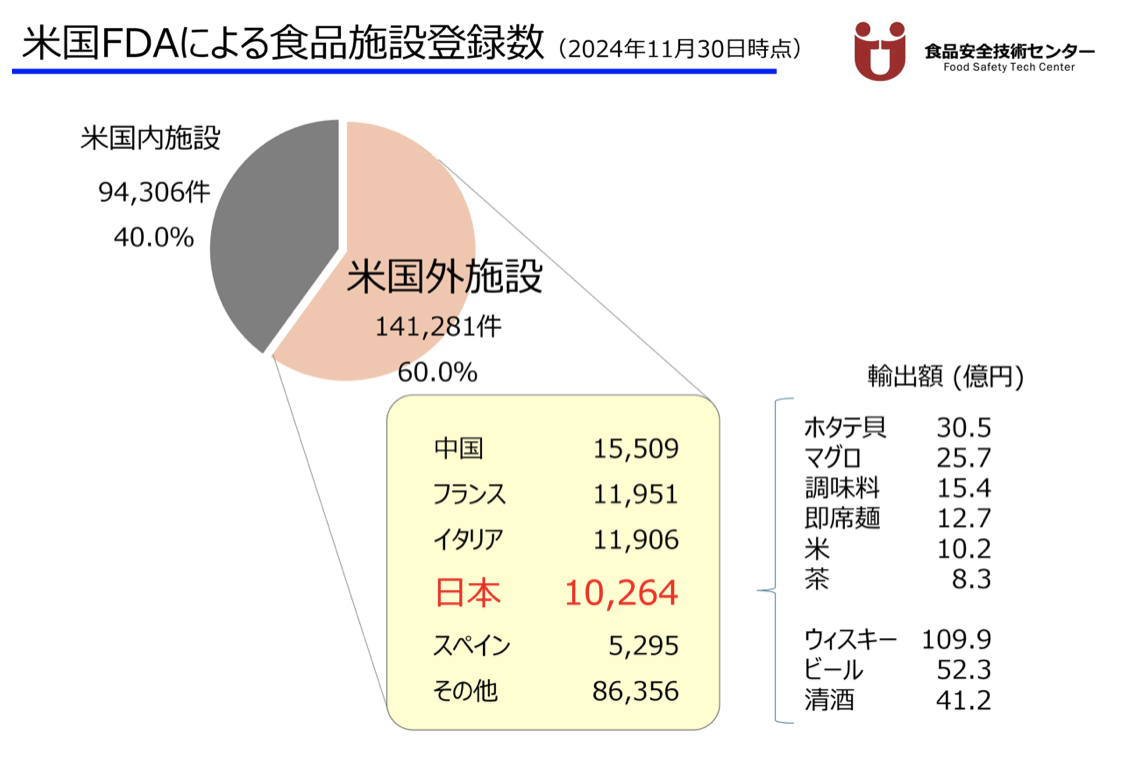
米国の食品安全情勢を見ると、2011年に予防的コントロール(Preventive Controls:PC)を基に法律が大幅に改定され、これはFood Safety Modernization Act(FSMA, 食品安全強化法)と呼ばれている。これは米国国内で流通する輸入食品(相手国)にも適用される。
具体的には、施設登録、資格者(PCQI:後述)の配置、それに基づく食品安全計画書の作成・運用が求められる。2020年7月にFDAは『New Era of Smarter Food Safety Bluepront』(10年間の計画)を公表し、中核的要素を1~4に分類し、テクノロジーを活用した安全で、デジタル化された追跡可能なシステムの構築を目指すとしている。日本の事業者もこの計画に迅速に対応する必要がある。
6. 米国食品安全強化法の主要条項と影響
FSMAの主要条項と影響としては、予防管理(第103条)、意図的汚染防止(第106条)、トレーサビリティ強化(第204条)がある。
予防管理を定める第103条では、食品施設に対してHARPC(Hazard Analysis and Risk-Based Preventive Controls:ハザード分析とリスクベースの予防管理)を義務付けており、これはHACCPを拡張した包括的なリスク管理アプローチとなる。
このHARPCを運用できる人をPCQIと呼ぶ。対象となるハザードでは、FDA年次リコール報告書によると、リコール事由の第1位が「アレルギー表示・管理(具体的には未申告アレルゲンの混入)」、第2位が「サルモネラ(死者数が多い)」、第3位が「リステリア・モノサイトゲネス(環境由来菌)」となっており、アレルギー表示と環境微生物管理を含めた広範囲のリスクに対する予防的管理が求められている。
第106条は意図的汚染防止(Food Defense)に関する規定で、「有資格者(qualified individual)を必要数配置」、「食品防御計画の作成」、「食品防御計画に基づく日々のモニタリング・検証・記録」がポイントとなる。
第204条はトレーサビリティ要件の強化を目的としており、Food Traceability List(FTL)掲載食品について、Key Data Elements(KDE)の電子的記録・共有が2028年7月から義務化される見込みである(正式決定は連邦官報での最終規則公布を待つ段階)。国外施設への査察も強化され、日本でも実施されている。2024年は日本企業108社(演者調べ)が査察を受けたが、今後は加速度的に増加することが予想される
7. 国内企業が取り組むべき課題と今後の方向性
国内食品企業が取り組むべき課題として、以下の点が挙げられる。
-
GFSI承認スキーム取得
GFSI承認スキームの取得による信頼確保とグローバル市場での競争力向上を目指す。 -
国際的要件への対応
FSMA・EU規制など国際要件への適応に加え、各国規制動向の把握と迅速な対応体制の構築が必要である。 -
デジタル技術の活用
IoT・ブロックチェーン活用による管理強化、リアルタイムモニタリングとトレーサビリティの向上を図る。 -
サプライチェーン全体での情報共有
トレーサビリティの向上と情報共有の推進、原材料から最終製品までの一貫管理、迅速な問題対応の実現が求められる。 -
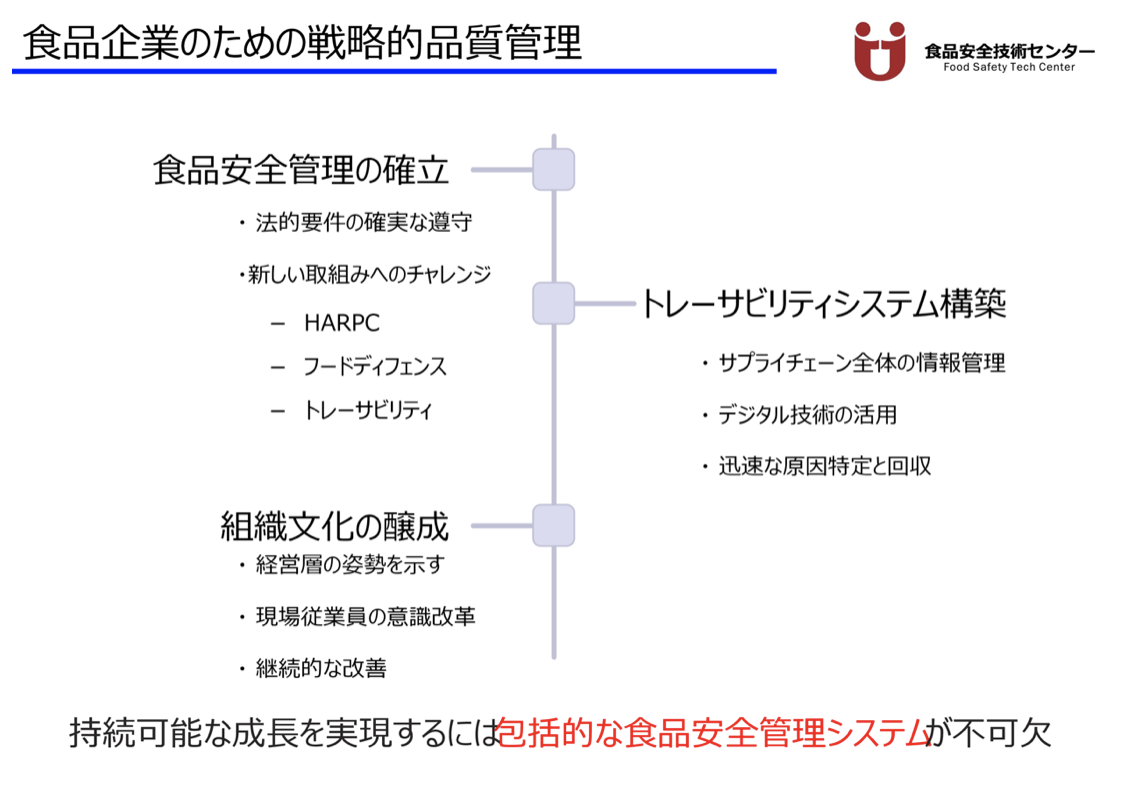
食品安全文化の醸成と組織全体への浸透
食品企業が持続可能な成長を実現するには、包括的な食品安全管理システムが不可欠である。
Q&A
Q2-1FSMAの影響で予防管理適格者(PCQI)を配置することなどが求められているが、実際にFDAの人間が査察に来る可能性について教えていただきたい。
A2-1対米輸出する場合には施設登録が必要であり、登録により査察対象となるが、FDAはリスクベースで査察対象を選定している。PCQIは工場ごとに置く必要はなく、施設に1人置けば良く、外部に依頼しても良いことになっている。
Q2-2対米輸出している企業は施設登録しているのか?
A2-23つのパターンが考えられる。一つは自社が登録してアメリカビジネスをしているパターンである。二つ目は間に入っている企業が登録しているパターンである。三つめは並行輸入会社である。
Q2-3現在、FSSC22000認証取得しているが、今後の会社としての進め方についてご意見をお聞かせいただきたい。
A2-3製品にマークを付けたいという考えがあれば、ISO17065の認証取得も一案である。ただし、マークの意味を消費者に伝えないと意味がない。
Q2-4AIの進化が著しいが、ハザード分析などで活用できると考えているが、何か知見などがあれば教えていただきたい。
A2-4例えば、特定のデータベースを読み込ませておいて、そのデータからしか情報を出力しない生成AI(例:NotebookLMのようなもの)がある。研究者であればz査読論文のデータを学習させておけば、そのデータに基づいてハザード分析ができるようになり、疫学データに基づいた分析が可能になると考えられる。
講演3
国際的に合意された科学的食品安全の枠組み
-汚染物質と残留農薬を例として-
山田 友紀子
International Food Safety Consultant
International Food Safety Consultant
1. はじめに~食品の「安全」とは~
食品中に存在し、健康被害をもたらす可能性のあるハザード(危害要因)は、生物学的ハザード(有害微生物や寄生虫など)、化学的ハザード(天然毒素や汚染物質、農薬、動物用医薬品、飼料添加物、添加栄養素・機能性成文、食品添加物、など)、物理的ハザード(日光や熱による変化や異物混入など)に分類される。
このうち化学的ハザードは極めて数が多く、新たに合成されたり、分析法の発展により新たに食品中から次々に検出されている状態である。化学物質は、食品中やそれを摂取した人の体内でより毒性の強い物質に代謝されたり変化したりすることはあるものの、微生物とは異なり食品中で勝手に著しく増殖することはない。また、化学物質の毒性や人の健康への悪影響について、安全性の評価やリスク評価は20世紀の初めから実施されてきている。
食品安全にかかわる化学的ハザードには、食料生産・製造に意図的に使用される結果として食品中に存在・残留する物質と、食品中の存在を意図していないにもかかわらず、食品中で自然に生成したり、食品成分が変化したり、環境中から汚染したりする物質がある。
前者の例としては、食品添加物、添加栄養素、機能性成分のように意図的に食品に使用され、食品中で機能を発揮するものや、農薬、動物用医薬品、飼料添加物のように作物や家畜に対して使用されるが、食品中の存在は意図されていないものがある。
これらのハザードのうち、意図的に食料生産・製造に使われる物質は、各国の政府により承認や登録(農薬の場合は「登録」という用語を使用)された化合物のみが、決められた食品・作物・家畜に、決められた方法でのみ使用できることになっている。それ以外の対象に、それ以外の方法で使用することは許されない。したがって、何か問題があっても管理や規制は、意図的に使用しない天然毒素や汚染物質より容易である。
また、食品の安全性は「量の問題」であることが非常に重要である。どのような物質や食品でも毒になりうるが、物質や食品が安全かどうかは、それらが体に吸収される量とそれぞれの毒性による。例えば、生命の維持に必要なビタミンA、鉄、食塩などでも、ある程度以上大量に摂取すれば、健康に悪影響が現れる。つまり、どのような量や濃度でも安全というものはないということである。
WTO加盟国の食品安全に関する措置は、科学的原則に則り、科学的根拠なしに維持してはならないとされており、行政=リスク管理機関には「科学」がなければならず、Codexの規格・基準が存在する場合にはそれに従うこととされている。Codexでは食品だけでなく飼料についても議論しており、これは飼料をコントロールしない限り、安全な肉や牛乳・卵などは得られないという考えに基づいている。
Codexにおいて汚染物質(カビ毒、細菌毒素、植物毒素、海藻毒素、重金属、有機化合物、放射性物質、農薬・動物用医薬品の残留など)とは、意図的に添加したわけではないのに存在するものと定義されており、偽装やバイオテロなどは含んでいない。

2. 食品中の天然毒素・汚染物質と残留農薬のリスク管理
これらハザードのリスク管理にはいくつかの措置がある。天然毒素・汚染物質の場合には、毒素の生成や汚染の防止・低減のための行動規範(GAP:Good Agricultural Practice, GMP:Good Manufacturing Practice, GHP:Good Hygienic Practiceなど)の設定と基準値の設定、消費者への勧告などがある。このうち食品の安全性向上に大きな役割を果たすのは前者である。
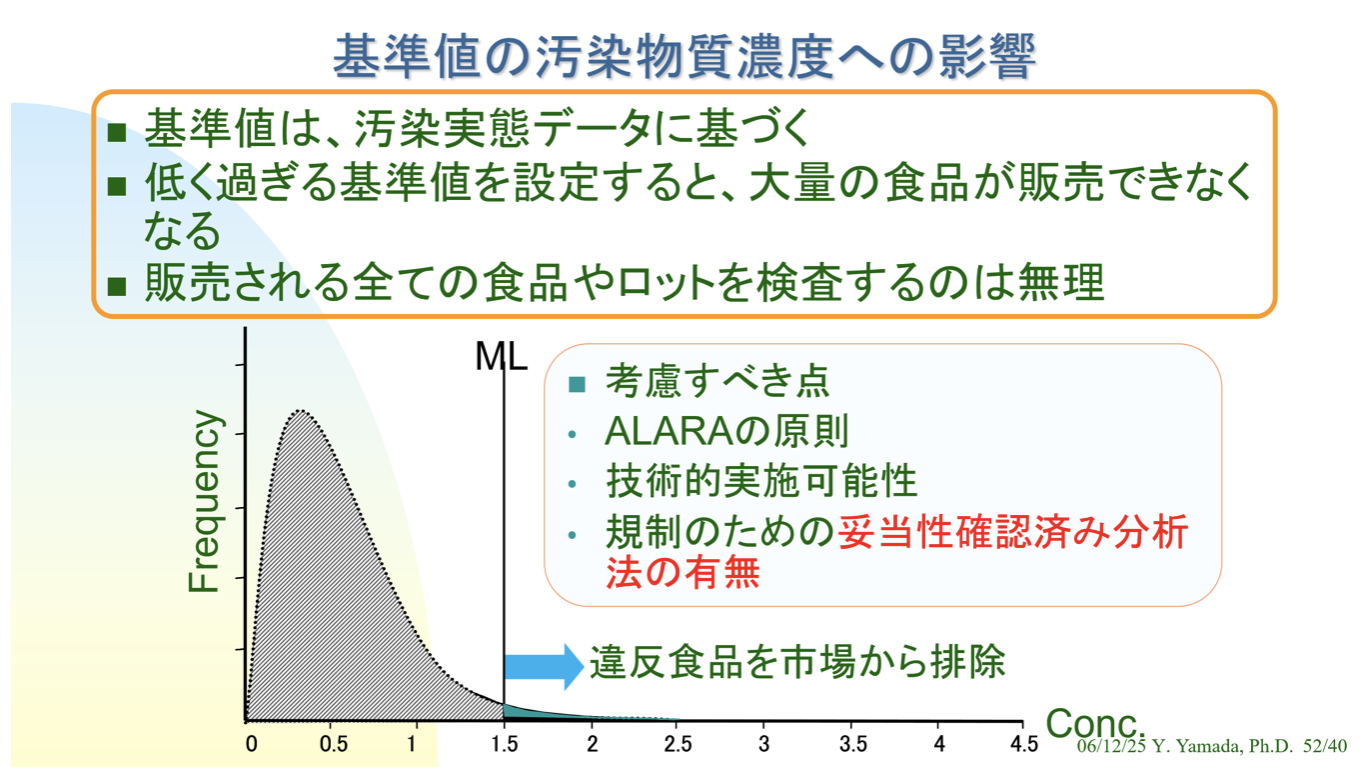
消費者への勧告も、リスク低減に有効である。基準値は食品自体を安全にする効果はないが、設定することにより、基準値を超える濃度で当該物質を含む食品を排除することができるし、国内でも日本への輸出国でも基準値に整合する製品の生産・製造が促進される。農薬については上記のように、登録制度が大きな役割を果たすが、基準値の設定もリスク管理措置の一つである。基準値の機能は天然毒素・汚染物質と同様である。
3. 汚染物質・残留農薬の基準値設定
リスク管理措置は科学的データに基づいて作成する義務があり、汚染物質については行動規範(汚染の防止と低減)と基準値がある。農薬に関しては、各国が実施する登録システムになっており、「登録された剤のみを、決められた作物にのみ、決められた方法でのみ使用できる」とされており、この中で使用基準(GAP)の設定がポイントとなっている。残留基準値を設定する目的は2つあり、一つは「使用基準(GAP)の遵守」、もう一つは「消費者の健康保護」である。
基準値の設定方法は、天然毒素・汚染物質と残留農薬では大きく異なる。いずれも、独立したリスク評価機関によるヒトの体内における代謝や毒性データの評価と、それによって導かれる毒性指標値(まとめてHealth-based Guidance Values、HBGVといい、Acceptable Daily IntakeやTolerable Daily Intake, Acute Reference Doseなどが含まれる)が必要である。
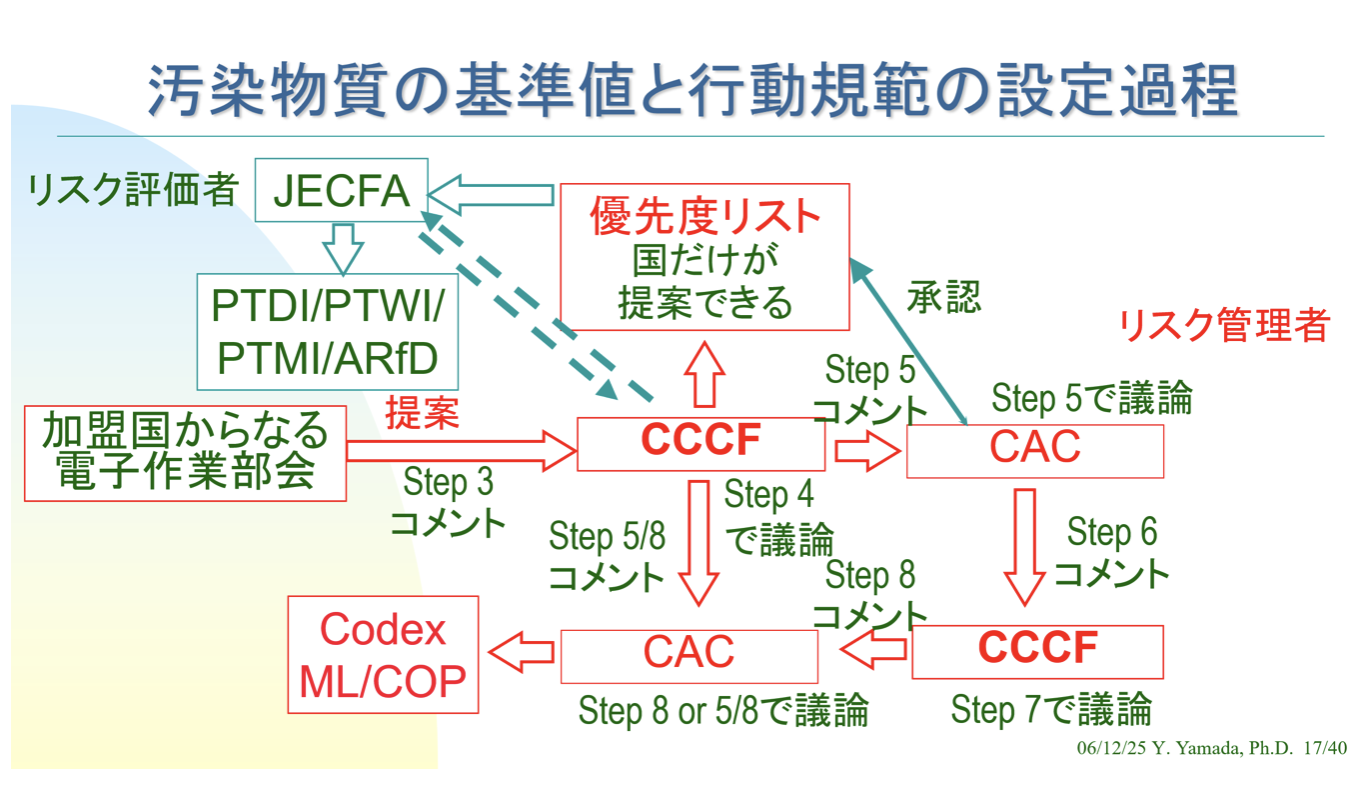
リスク管理機関であるCodexにおいて、天然毒素・汚染物質の場合は、Codex Committee on Contaminants in Food(CCCF)内の電子作業部会が、各国からGEMS/Foodを通じて提供された汚染実態データを解析して基準値案を作成する。
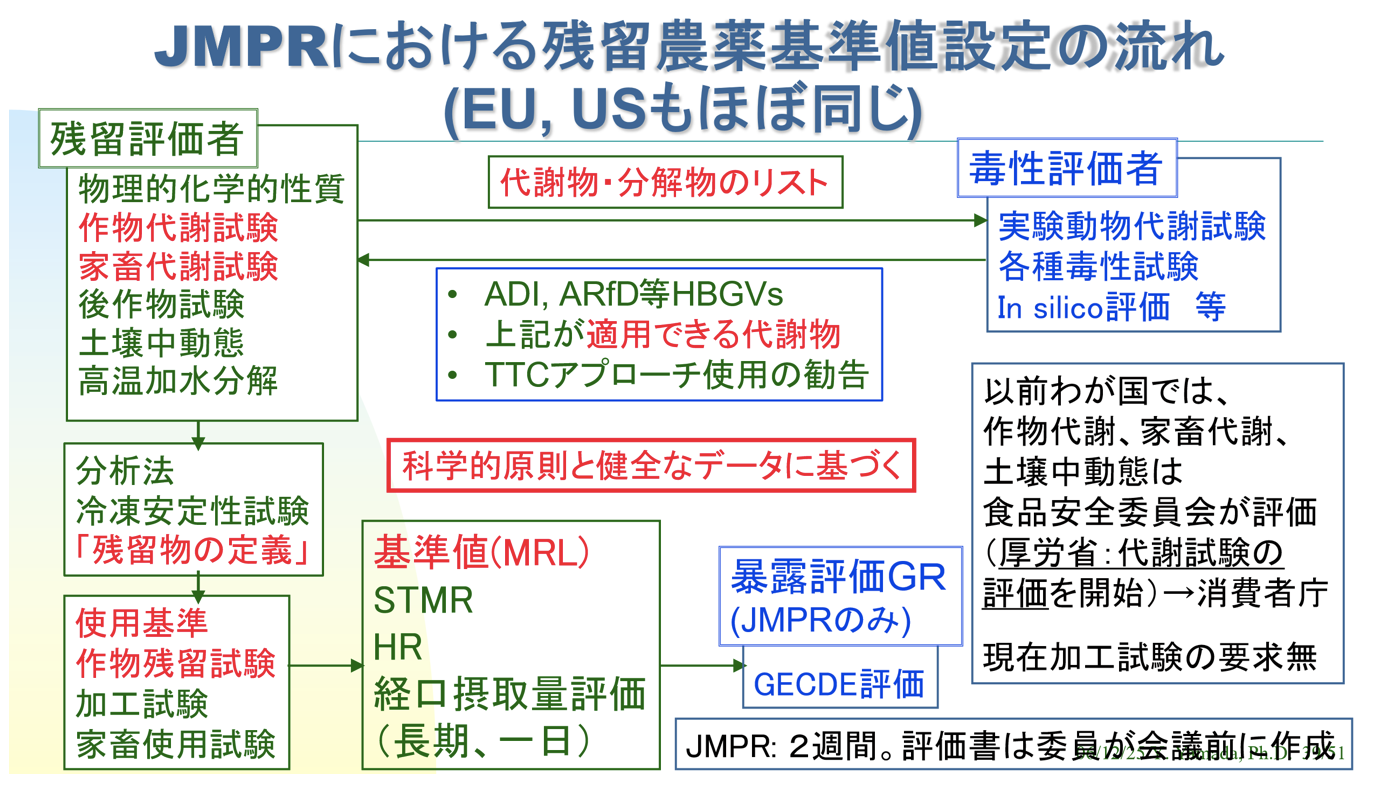
一方、残留農薬の場合はCodexから独立したリスク評価機関であるJoint FAO/WHO Meeting on Pesticide Residues(JMPR)のFAOパネルが、通常農薬メーカーから提出された代謝、環境動態、作物残留、加工、動物飼養等の試験結果や分析法、冷凍安定性に関するデータを評価して基準値案をCodex Committee on Pesticide Residuesに提案する。
基準値設定の原理・原則として、消費者の健康保護のために十分低くなければならないとされる一方、適正な生産・製造等をしている生産者・製造者等を守るため、また検査で定量できるようにするために十分高くなければならないとされる。
さらに、これらのデータの作成には、統計的なサンプリング法、妥当性確認された分析法(適切な定量下限値を持つ必要)、品質保証制度を導入している分析機関における分析などの要件を満たす必要があり、分析結果の精査と、統計学的解析により基準値案と摂取量評価をすることが必要となる。
基準値には食品を安全にする機能はなく、安全性を判断するためには経口摂取量を推定し、毒性指標値と比較しなければならない。基準値は一定の違反があるように策定する必要がある。
健康リスクの要因には、「毒性の特性」、「摂取期間」、「経口摂取量」があり、経口摂取量評価に必要なデータには、ハザードの濃度、関連食品消費量があり、加工・調理による濃度変化のデータがあればなお良い。経口摂取量評価の方法には、「一点推計」と「確率論的推計」がある。食品の基準値設定を設定すれば、規制と検査が必須になることに留意する。
4. 生産・製造法の改善
GAP、GMP、GHPなどの行動規範は、食品の安全性を向上させるために実施するものであり、フードチェーンアプローチの原則に則っている。現実に有効なものを作成するためには他省庁や業界との連携が必須である。実そして施後は、措置の有効性の検証と見直しが必要である。例えば、USFDAでは基準値を設定したら、それに整合するためのCode of Practiceも策定している。
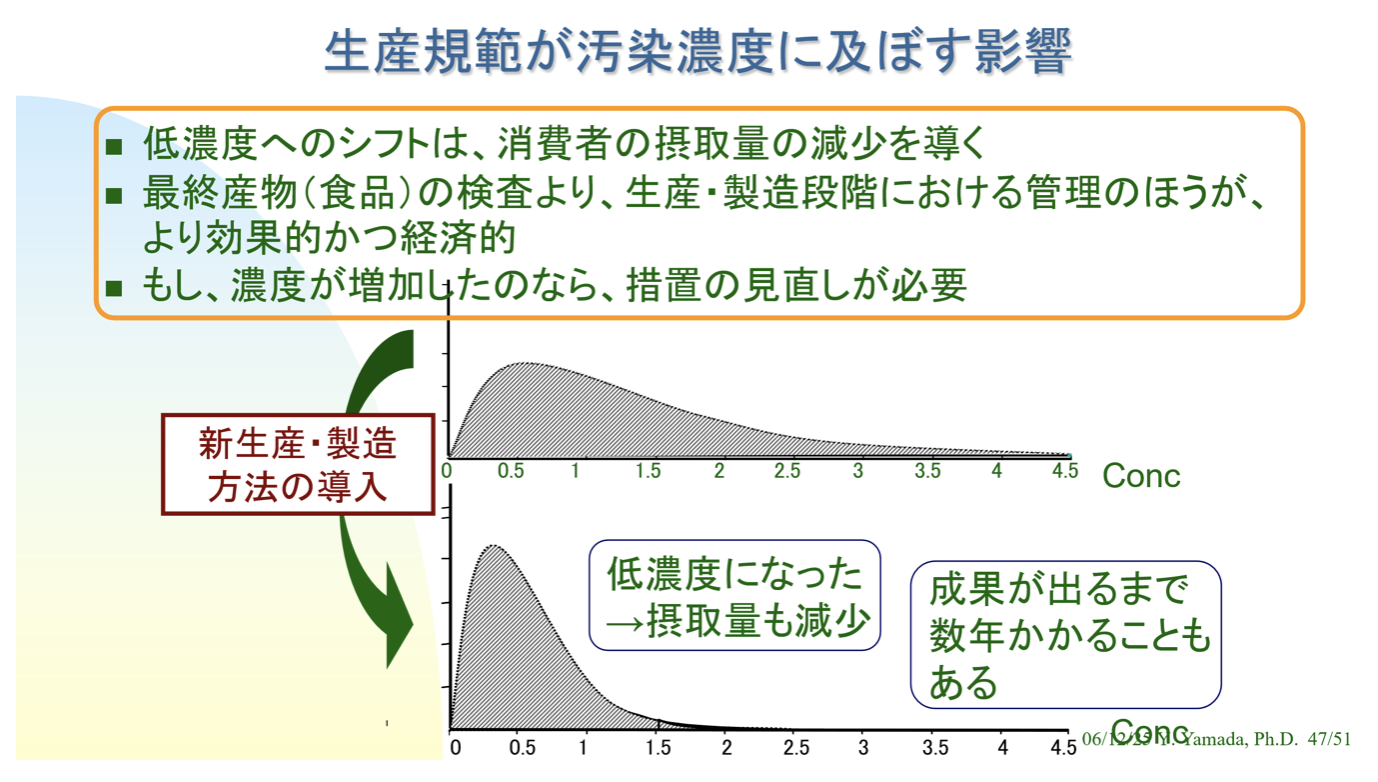
5. 提案
天然毒素・汚染物質については、何か問題が発生するのを待つのではなく、国だけでなく民間機関においても汚染実態データを収集し、基準値または目標値等を設定することが有用であると考える。ただし、その際には統計学的サンプリングを実施すること、妥当性確認された適切な定量下限値を持つ分析法により品質保証制度を導入している分析機関で分析されたデータであることが前提となる。
残留農薬については、新規剤の基準値の評価だけでなく、CodexやJMPRなどのように再評価を実施する必要がある。その際には国際的な評価方法を使用すべきであるし、重要な食品に関しては加工試験の導入も必要であると考える。
Q&A
Q3-1残留農薬について基準を超過したことが判明した際には、原料をたどりどのような管理をしていたか見つけることが良いのか?また検査対象として加工品を想定した場合、原料をたどって検査した方が良いのか?
A3-1基準値を超過していることが判明した場合、やるべきことは2つある。まず暴露評価(摂取量の評価)が必要となる。もう一つは原因を探ることである。検査対象としては、国際的には原料あるいは単一の原料からできた食品が対象となっている。例えば100%果汁ジュースやペーストのように単一原料から製造される加工品では基準値の設定も可能だが、レトルトのカレーのように複数原料から成る加工品では、何に何がどれくらい入っているか不明であるため基準値の設定は難しい。
